Genetica glioamelor – de la biologie moleculară la decizie terapeutică
Introducere
Glioamele reprezintă un grup heterogen de tumori primare ale sistemului nervos central, caracterizate nu doar prin aspect histologic, ci mai ales printr-un profil molecular distinct. În ultimele două decenii, genetica glioamelor a devenit esențială în înțelegerea comportamentului biologic al acestor tumori și în alegerea tratamentului optim.
Clasificarea modernă, bazată pe criteriile OMS (WHO 2021), nu mai separă tumorile exclusiv după morfologie, ci integrează modificările genetice și epigenetice. Astfel, diagnosticul de „gliom” este astăzi incomplet fără analiza moleculară.
Conceptul de gliom: o boală genetică
Glioamele nu sunt doar tumori care cresc necontrolat, ci rezultatul acumulării progresive de mutații genetice în celulele gliale sau în precursorii acestora.
Aceste mutații determină:
- activarea oncogenelor
- inactivarea genelor supresoare tumorale
- dereglarea ciclului celular
- alterarea mecanismelor de reparare ADN
- modificări epigenetice persistente
În esență, genetica glioamelor reflectă un dezechilibru între proliferare și controlul celular.
Clasificarea moleculară a glioamelor
Astăzi, glioamele difuze sunt împărțite în trei mari categorii, definite genetic:
- gliom difuz IDH-mutant (astrocytom)
- oligodendrogliom IDH-mutant și 1p/19q codeletat
- glioblastom IDH-wildtype
Această clasificare este fundamentală deoarece fiecare tip are:
- evoluție diferită
- răspuns diferit la tratament
- prognostic distinct
Mutațiile IDH – cheia înțelegerii glioamelor
Mutațiile în genele IDH1 și IDH2 reprezintă unul dintre cele mai importante evenimente genetice în glioamele difuze.
Aceste mutații:
- apar precoce în oncogeneză
- sunt prezente în majoritatea glioamelor de grad scăzut
- sunt asociate cu prognostic mai bun
Mecanismul este unul fascinant: enzima IDH mutantă produce un metabolit anormal (2-hidroxiglutarat), care determină modificări epigenetice profunde.
Consecințe:
- hipermetilare ADN
- blocarea diferențierii celulare
- menținerea celulelor într-o stare „stem-like”
Codeleția 1p/19q – semnătura oligodendrogliomului
Oligodendroglioamele sunt definite prin asocierea dintre:
- mutația IDH
- codeleția brațelor cromozomiale 1p și 19q
Această modificare genetică are implicații majore:
- răspuns excelent la chimioterapie (PCV)
- sensibilitate crescută la radioterapie
- supraviețuire prelungită
Este una dintre cele mai clare corelații între genetică și prognostic în neuro-oncologie.
TP53 și ATRX – caracteristice astrocitoamelor
Astrocitoamele IDH-mutante prezintă frecvent:
- mutații TP53
- pierderea expresiei ATRX
Rolul acestor gene:
- TP53 controlează apoptoza și stabilitatea genomică
- ATRX este implicată în menținerea telomerilor
Pierderea ATRX duce la mecanismul ALT (alternative lengthening of telomeres), care permite celulelor tumorale să se dividă indefinit.
Glioblastomul IDH-wildtype – agresivitate genetică
Glioblastomul clasic (IDH-wildtype) este caracterizat printr-un profil genetic complet diferit:
- amplificare EGFR
- mutații TERT promoter
- pierdere PTEN
- alterări ale cromozomului 7 și 10
Aceste modificări determină:
- proliferare rapidă
- invazivitate crescută
- rezistență la tratament
EGFR – motorul proliferării tumorale
Amplificarea receptorului EGFR este una dintre cele mai frecvente modificări în glioblastom.
Consecințe:
- activarea căilor de semnalizare proliferative
- creșterea angiogenezei
- inhibarea apoptozei
Variantele mutante, precum EGFRvIII, sunt asociate cu un comportament biologic agresiv.
Promotorul TERT – nemurirea celulară
Mutațiile promotorului TERT duc la activarea telomerazei, o enzimă care:
- previne scurtarea telomerilor
- permite diviziuni celulare infinite
Această modificare este prezentă în:
- majoritatea glioblastoamelor
- oligodendroglioame
MGMT – predictorul răspunsului la tratament
Metilarea promotorului MGMT este una dintre cele mai importante modificări predictive.
MGMT este o enzimă care repară ADN-ul după chimioterapie.
Dacă promotorul este metilat:
- enzima nu mai este produsă
- tumora devine mai sensibilă la temozolomid
Implicație clinică:
- pacienții cu MGMT metilat au răspuns mai bun la tratament
Alterări ale căilor de semnalizare
În glioame sunt afectate multiple căi intracelulare:
1. Calea RTK/RAS/PI3K
- activată prin EGFR
- duce la proliferare și supraviețuire celulară
2. Calea p53
- afectează controlul ciclului celular
- permite acumularea de mutații
3. Calea RB
- reglează tranziția G1-S
- alterarea duce la proliferare necontrolată
Epigenetica în glioame
Pe lângă mutațiile genetice, epigenetica joacă un rol major.
Fenomenul G-CIMP (glioma CpG island methylator phenotype):
- caracteristic glioamelor IDH-mutante
- asociat cu prognostic favorabil
Epigenetica influențează:
- expresia genelor
- răspunsul la tratament
- evoluția tumorii
Heterogenitatea tumorală
Un aspect esențial al glioamelor este heterogenitatea:
- diferențe între zone ale aceleiași tumori
- subclone genetice multiple
- evoluție în timp
Aceasta explică:
- recurența tumorilor
- rezistența la tratament
- dificultatea eradicării complete
Evoluția genetică a glioamelor
Glioamele evoluează prin acumularea progresivă de mutații.
Exemplu:
- gliom IDH-mutant de grad scăzut
→ acumulare mutații suplimentare
→ transformare în grad înalt
Acest proces se numește progresie malignă
Biomarkeri moleculari în practică
Astăzi, diagnosticul complet al unui gliom include:
- IDH1/IDH2
- 1p/19q
- ATRX
- TP53
- MGMT
- TERT
- EGFR
Acestea sunt esențiale pentru:
- stabilirea diagnosticului
- alegerea tratamentului
- estimarea prognosticului
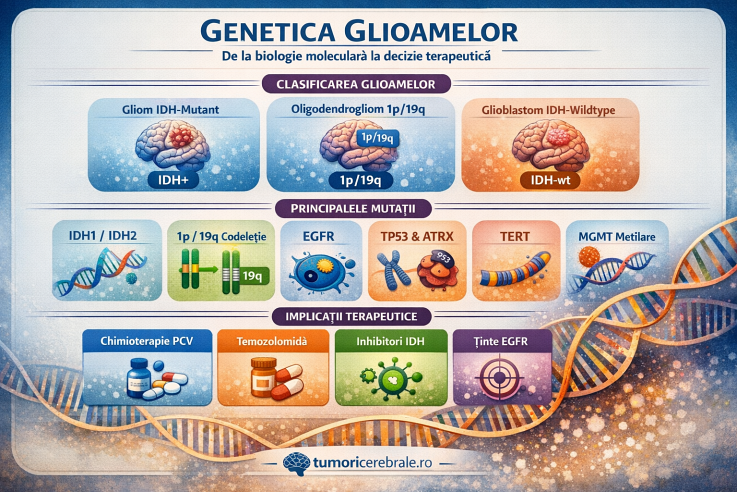
Implicații terapeutice
Genetica glioamelor influențează direct tratamentul:
- IDH-mutant → prognostic mai bun
- 1p/19q → sensibilitate la PCV
- MGMT metilat → răspuns la temozolomid
- EGFR → posibilă țintă terapeutică
Se dezvoltă terapii țintite:
- inhibitori IDH
- terapii anti-EGFR
- imunoterapie
Terapia personalizată
Viitorul tratamentului în glioame este personalizat:
- bazat pe profil genetic individual
- adaptat la fiecare pacient
- orientat spre medicina de precizie
Limitările actuale
Deși genetica a revoluționat domeniul, există limitări:
- heterogenitatea tumorală
- barierele hemato-encefalice
- lipsa unor terapii țintite eficiente pe scară largă
Perspective viitoare
Direcțiile de dezvoltare includ:
- secvențiere genomică extinsă
- inteligență artificială în interpretare
- terapii combinate
- vaccinuri tumorale
Concluzie
Genetica glioamelor a schimbat fundamental modul în care înțelegem aceste tumori. Nu mai vorbim doar despre „ce vedem la microscop”, ci despre un profil molecular complex care dictează evoluția bolii.
Pentru pacient, acest lucru înseamnă:
- diagnostic mai precis
- tratament mai bine adaptat
- șanse mai bune pe termen lung
Pentru medic, genetica devine un instrument esențial în luarea deciziilor terapeutice.
| Caracteristică | 🟦 Astrocitom IDH-mutant | 🟩 Oligodendrogliom (1p/19q) | 🟥 Glioblastom IDH-wildtype |
|---|---|---|---|
| Profil genetic cheie | IDH + TP53 + ATRX | IDH + 1p/19q | EGFR + TERT |
| Mutație IDH | ✔️ | ✔️ | ❌ |
| Codeleție 1p/19q | ❌ | ✔️ (definitorie) | ❌ |
| TP53 | ✔️ frecvent | ❌ rar | ⚠️ variabil |
| ATRX | ❌ pierdut | ✔️ păstrat | ⚠️ variabil |
| TERT promoter | ❌ rar | ✔️ frecvent | ✔️ frecvent |
| EGFR | ❌ rar | ❌ rar | ✔️ amplificat |
| MGMT metilare | ✔️ frecvent | ✔️ frecvent | ⚠️ variabil |
| Mecanism telomeric | ALT (ATRX) | Telomerază | Telomerază |
| Grad OMS | II–III (± IV) | II–III | IV |
| Vârstă tipică | 30–50 ani | 30–50 ani | >60 ani |
| Evoluție | 🟦 Lentă | 🟩 Lentă | 🟥 Rapidă |
| Sensibilitate la tratament | 🟦 Moderată | 🟩 Foarte bună | 🟥 Redusă |
| Răspuns la chimioterapie | ✔️ | ✔️✔️ (excelent) | ⚠️ limitat |
| Prognostic | 🟦 Intermediar | 🟩 Favorabil | 🟥 Nefavorabil |
| Supraviețuire medie | 5–15+ ani | 10–20+ ani | 12–18 luni |
| Semnătură biologică | Instabilitate controlată | Tumoră „sensibilă” | Agresivitate moleculară |