Despre Glioblastom
Glioblastomul este o tumoră cerebrală malignă, cea mai des întâlnită și cea mai agresivă dintre toate. Ea nu se dezvoltă din neuroni, celulele nervoase propriu-zise, ci din celulele gliale (celulele de suport ale sistemului nervos central). Acestea au multiple roluri în susținerea și hrănirea neuronilor, cât și în izolarea electrică a fibrelor nervoase. Celulele gliale sunt de aproximativ zece ori mai numeroase decât neuronii și, spre deosebire de aceștia, se divid și pot da naștere la tumori, benigne sau maligne.
Cum se clasifică tumorile gliale?
Tumorile gliale se împart în astrocitoame (derivate din astrocite, cele mai numeroase celule gliale și cele mai frecvente tumori) și oligodendroglioame (derivate din oligodendrocite, un subtip mai puțin numeros de celule gliale).
Din punct de vedere al agresivității, există patru grade:
- Grad I – tumorile benigne – astrocitomul pilocitic. Apare în special la copii și are un prognostic foarte bun.
- Grad II – tumorile benigne, dar cu potențial de malignizare – astrocitomul fibrilar și gemistocitic, oligodendrogliomul, xantoastrocitomul pleomorf. Sunt tumori care infiltrează țesutul cerebral normal și, în timp, evoluează spre tumori maligne.
- Grad III – astrocitomul anaplazic și oligodendrogliomul anaplazic. Sunt tumori maligne, dar nu atât de agresive precum glioblastomul.
- Gradul IV – glioblastomul – tumoră malignă, cea mai agresivă formă de tumoră cerebrală a adultului.
De câte feluri sunt glioblastoamele?
Există două forme principale de glioblastom, diferența dintre ele fiind făcută de modul de apariție și evoluție. Desigur, în spatele acestor diferențe stau mutații genetice distincte, caracteristice fiecărui subtip.
- Glioblastomul primar care apare de la bun început ca o tumoră malignă, agresivă, evoluează rapid și răspunde prost la radioterapie și chimioterapie.
- Glioblastomul secundar care apare inițial ca o tumoră de gradul II (astrocitom fibrilar), evoluează mult timp asimptomatică și se transformă cu timpul într-un astrocitom anaplazic (grad III) și apoi în glioblastom (grad IV). Răspunsul la radioterapie și chimioterapie este mult mai bun decât în cazul glioblastomului primar.
Mutațiile genetice din glioblastom
Celula tumorală din glioblastom este o celulă care se divide necontrolat și este capabilă să supraviețuiască în medii ostile cu pH acid și concentrație scăzută de oxigen. De asemenea, aceasta poate rezista la radioterapie și la citostatice sau poate cauza producerea de noi vase de sânge. Toate aceste caracteristici se datorează prezenței unor mutații genetice în ADN-ul celulei maligne, mutații responsabile de caracterul biologic al tumorii. Există numeroase gene mutante descoperite în celulele de glioblastom, câteva dintre ele fiind mai importante, precum:
p53 – gena care oprește celula să se dividă. Formele mutante sunt nefuncționale.
VEGF-R – factorul de creștere vascular care determină producerea de noi vase de sânge pentru tumoră.
EGF-R – factorul de creștere epitelial care stimulează diviziunea celulară.
De ce apare glioblastomul?
![]()
Nu se cunoaște o cauză de apariție a glioblastomului. Există unele rare sindroame genetice (Li-Fraumeni, neurofibromatoza), însă majoritatea cazurilor sunt sporadice, fără transmitere genetică.
Expunerea la substanțe toxice sau la radiații ionizante poate cauza o asemenea tumoră, însă, la fel, aceste cazuri sunt rare.
Cum se manifestă?
Glioblastomul este o tumoră cu creștere rapidă. De la stadiul de celulă malignă până la cel de tumoră cu manifestări clinice pot trece chiar și doar câteva luni.
Cel mai adesea, primul simptom este durerea de cap, datorată creșterii presiunii intracraniene.
Deficitele neurologice depind de localizarea tumorii. Cele mai frecvente sunt hemipareza (scăderea forței musculare) pe partea opusă, tulburările de limbaj (când tumora este pe partea stângă la dreptaci și pe dreapta la stângaci), tulburările de memorie (lobul temporal) și modificarea câmpului vizual (lobii temporali sau occipitali). Inițial, acestea se datorează edemului cerebral care însoțește tumora, și sunt reversibile cu tratament medicamentos (Dexametazonă sau Medrol) sau prin operație. Când se datorează invaziei tumorale, deficitele sunt mai accentuate și definitive.
În stadiile avansate, cu tumori de mari dimensiuni și hipertensiune intracraniană apar și tulburări psihice sau, în stadiile finale, somnolență și comă. Tot din cauza creșterii presiunii intracraniene poate apărea edem papilar cu scăderea vederii; diagnosticul se stabilește prin consult oftalmologic (examenul fundului de ochi).
Crizele de epilepsie pot fi o altă manifestare a glioblastomului și pot îmbrăca foarte multe forme, în funcție de localizare. Pot fi cu, sau fără pierderea conștienței, cu manifestări motorii (convulsii) sau de altă natură, inclusiv modificări neuropsihice și de comportament (crizele temporale).
Cum se pune diagnosticul?
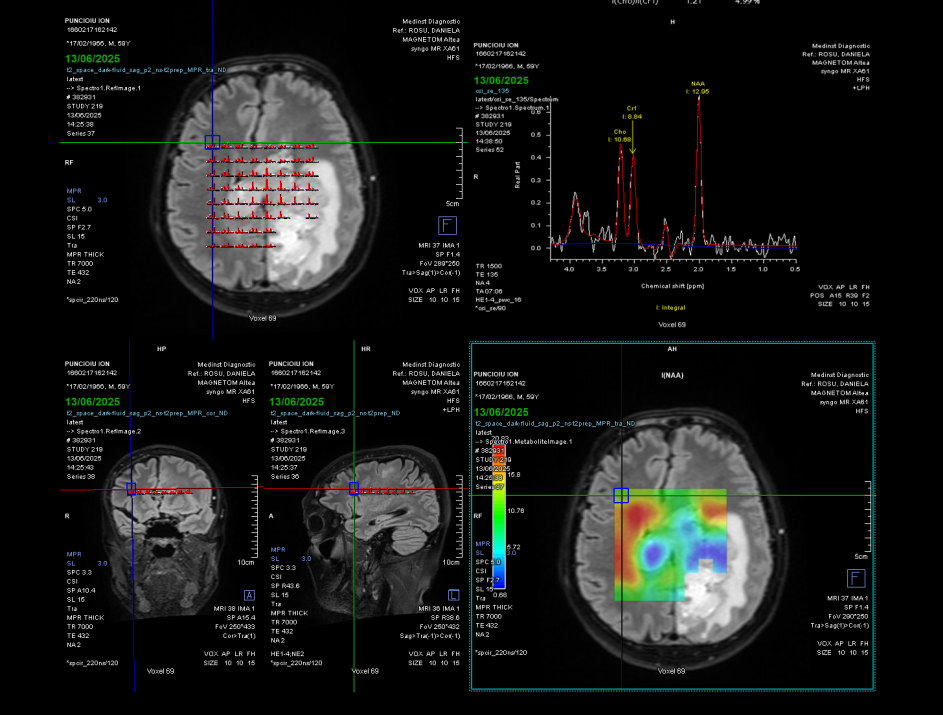
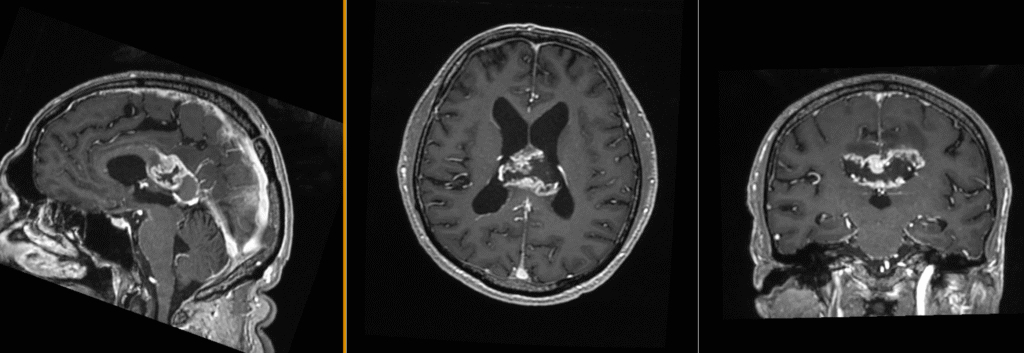
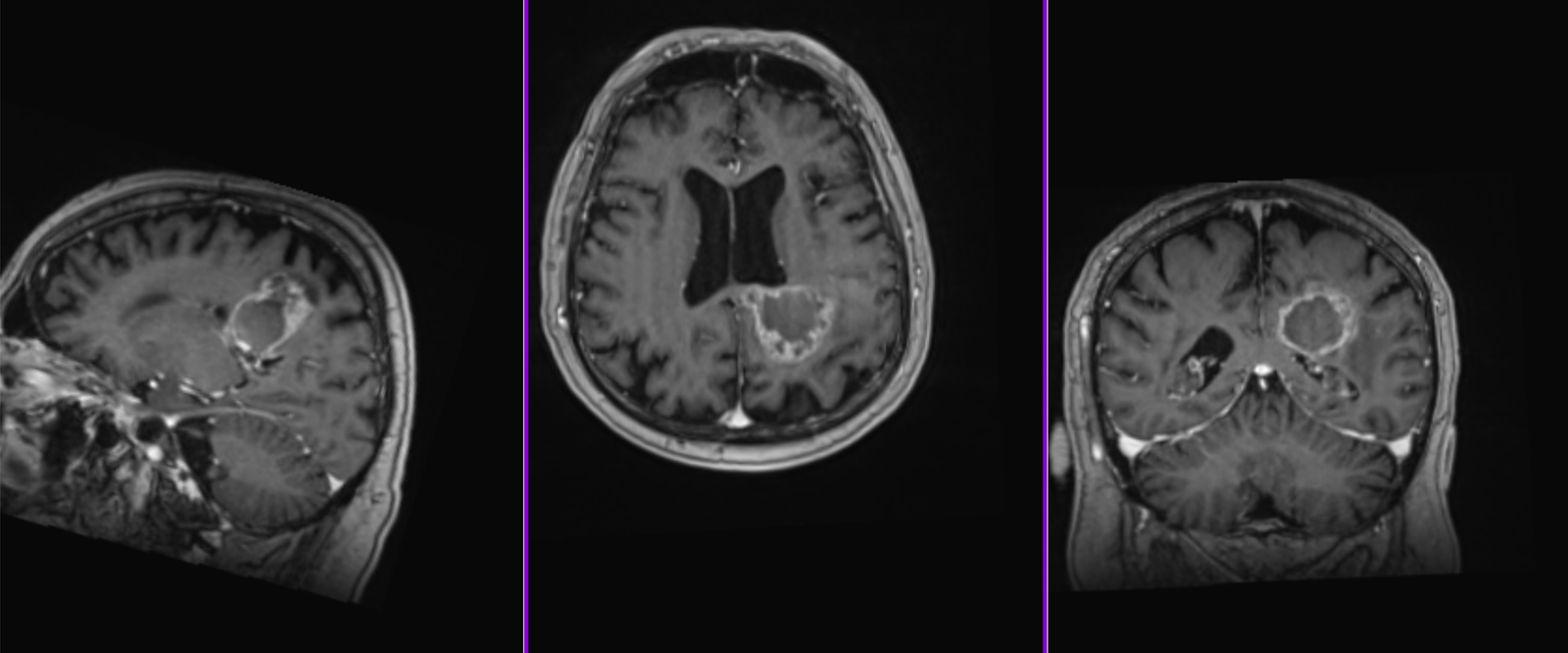
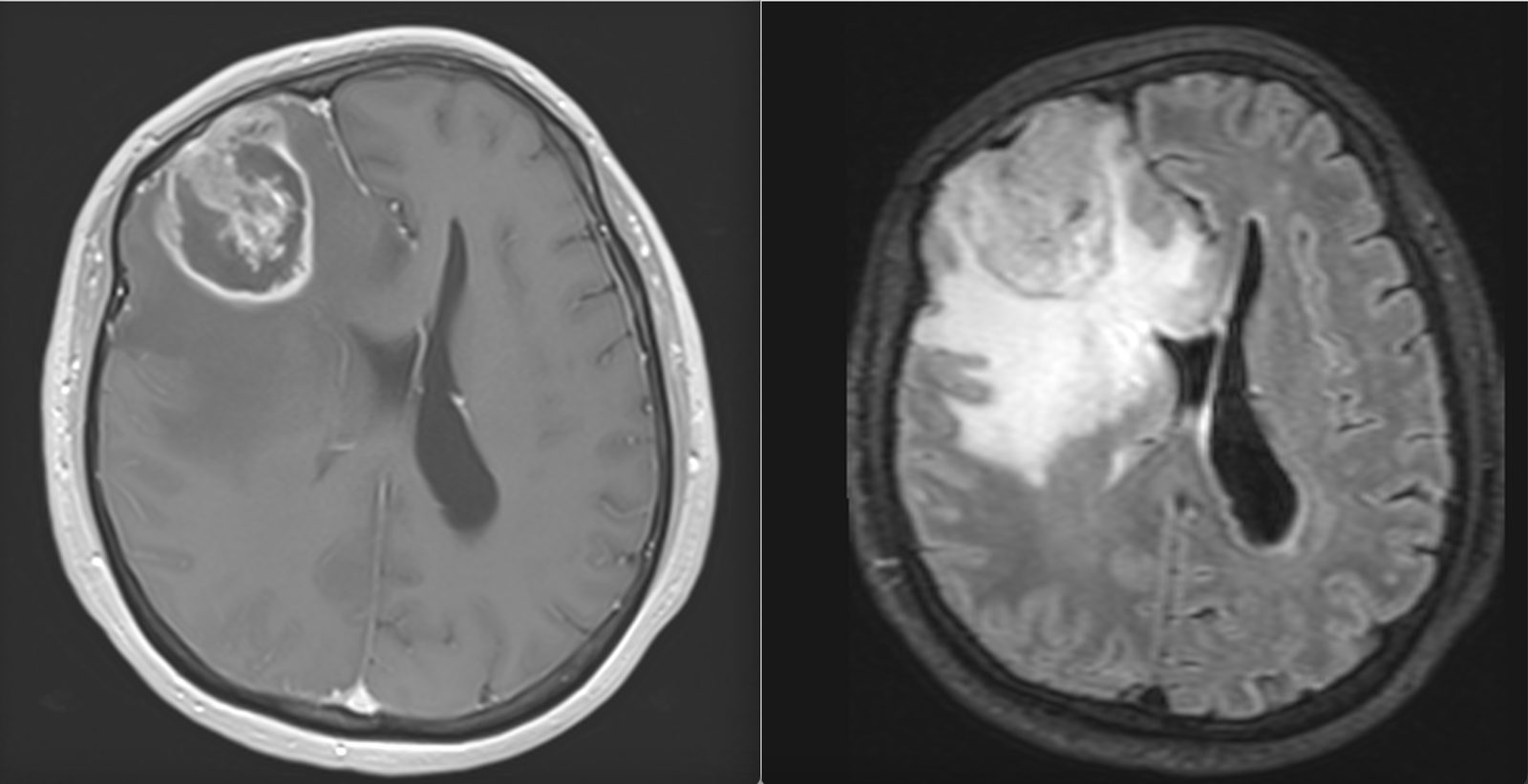
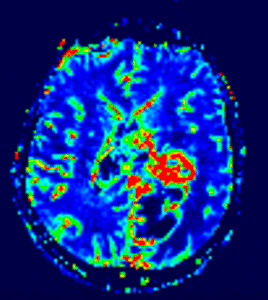
Diagnosticul se pune prin rezonanță magnetică (RMN) sau computer-tomograf (CT) cu substanță de contrast. Glioblastomul apare ca o tumoră dezvoltată în interiorul creierului, prost delimitată, cu priză de contrast, edem în creierul din jur și, de multe ori, cu zone de necroză care nu captează substanța de contrast.
Diagnosticul pe baza RMN-ului este de probabilitate, cel definitiv, de certitudine, stabilindu-se prin examen anatomopatologic și imunohistochimic. Acesta se face fie pe tumora îndepărtată chirurgical, fie pe fragmente de tumoră recoltate prin biopsie.
Biopsia cerebrală presupune recoltarea unui fragment de tumoră printr-o procedură minimă, cu ajutorul unui ac special. Se poate face fie prin stereotaxie, fie cu ajutorul neuronavigației. Aceasta din urmă este mai puțin precisă, dar mai simplă ca procedură și mai ușor de tolerat de către pacient.
Nu există analize de sânge (markeri sanguini) pentru glioblastom.
Cum evoluează glioblastomul?
Glioblastomul este o tumoră cu creștere rapidă. Celulele tumorale sunt foarte mobile și infiltrează țesutul cerebral din jur, de-a lungul fibrelor din substanța albă. Astfel, există forme de glioblastom care la momentul diagnosticului este deja extins în ambele emisfere cerebrale (glioblastom în fluture). Crescând în dimensiuni, tumora determină creșterea presiunii intracraniene, ceea ce determină cefalee (dureri de cap) și alterarea progresivă a stării neurologice, mergând de la stare confuzională și tulburări de comportament până la comă profundă în formele avansate.
Deficitele neurologice (pareze, tulburări de vorbire etc.) sunt inițial datorate edemului cerebral și sunt reversibile. Cu toate acestea, pe măsură ce tumora crește se produce o distrugere definitivă a centrilor nervoși și a conexiunilor dintre ei, ceea ce înseamnă că deficitele neurologice devin permanente.
Care sunt posibilitățile de tratament?
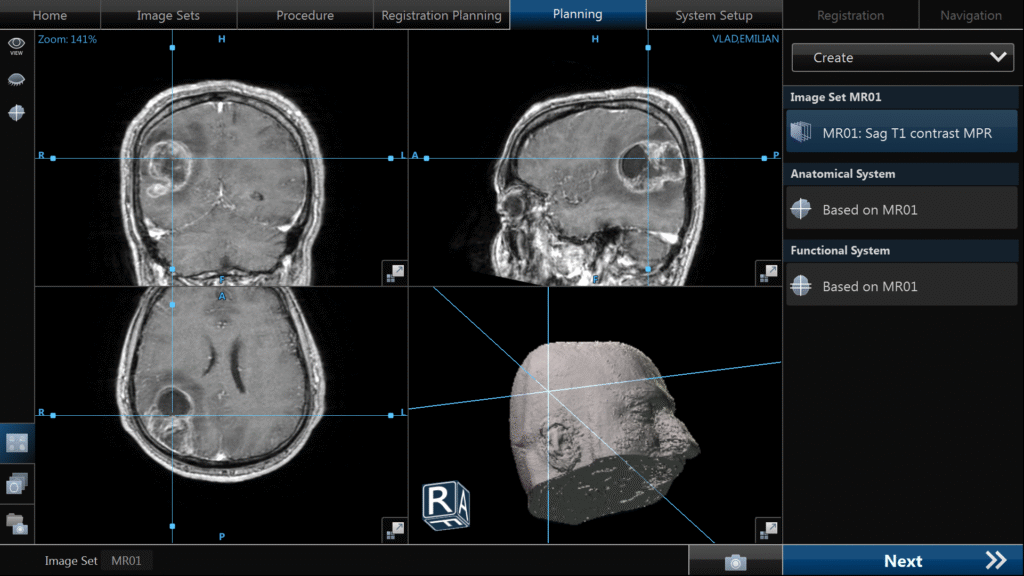
Tratamentul glioblastomului este multimodal, adică include mai multe metode terapeutice.
Tratamentul chirurgical este prima linie de tratament în majoritatea cazurilor. Prin operație vizăm îndepărtarea cât mai completă a tumorii, fără însă a provoca deficite neurologice noi (hemipareză, tulburări de vorbire etc.). Atunci când nu putem îndepărta tumora în totalitate se face rezecție parțială sau doar o biopsie în scopul stabilirii diagnosticului histopatologic.
Tratamentul chirurgical modern al glioblastomului presupune utilizarea neuronavigației, a disectorului ultrasonic și a fluorescenței intraoperatorii cu acid 5-amino levulinic (5-ALA). Aceste dotări sunt necesare pentru îndepărtarea cât mai completă a tumorii.
Din cauza caracterului infiltrativ al glioblastomului, cu celule care migrează în țesutul cerebral normal înconjurător, nu se poate obține o ablație completă în adevăratul sens al cuvântului, însă este posibilă îndepărtarea totală a porțiunii solide, compacte. Cu cât restul tumoral este mai redus, cu atât supraviețuirea este mai bună, însă doar dacă se poate îndepărta minimum 90% din tumoră.
Radioterapia este obligatorie pentru glioblastom și se începe la 3-4 săptămâni după operație. Se iradiază atât locul unde s-a aflat tumora, precum și creierul din jur unde există celule tumorale migrate. Se folosește o doză de 56-60 Gy care se administrează în doze zilnice de 1,8-2,0 Gy. Tratamentul durează în medie 6 săptămâni (30 ședințe, câte 5 pe săptămână) și este în general bine suportat, având puține efecte adverse. Căderea părului și amețelile sunt cele mai frecvente. De asemenea, radioterapia poate cauza edem cerebral, motiv pentru care se administrează concomitent Dexametazonă sau Medrol/Solumedrol.
Ca și tehnologie de radioterapie, se folosește iradierea conformațională, cu variantele mai moderne – IMRT și VMAT; Gamma-Knife sau Cyberknife nu sunt eficiente în cazul glioblastomului.
Chimioterapia citostatică este, de asemenea, obligatorie și se administrează concomitent cu radioterapia și, ulterior, în cure de trei zile în fiecare lună. Citostaticul de primă intenție este Temozolamida (Temodal – denumirea comercială) și se administrează pe cale orală, fiind bine tolerat de către pacienți.
În linia a doua de tratament citostatic se află Irinotecanul și Avastinul, precum și medicamentele de generație mai veche – Procarbazina, Lomustina și Vincristina.
Există foarte multe studii clinice dedicate glioblastomului cu numeroase terapii biologice, imunologice și genetice, însă, în prezent, acestea se află în stadiul de trialuri clinice, neconfirmate și nerecomandate pentru tratamentul curent.
Când trebuie făcută operația?
Deoarece glioblastomul este o tumoră agresivă, cu creștere rapidă, operația trebuie făcută cât mai rapid după stabilirea diagnosticului prin RMN. Atunci când tumora poate fi extirpată, efectuarea unei biopsii înainte este inutilă, cauzând astfel întârzierea tratamentului.
În funcție de dimensiunea tumorii, de starea generală și de cea neurologică a pacientului se poate aștepta până la 2-3 săptămâni, însă, cu cât se intervine chirurgical mai devreme cu atât este mai bine.
Dacă au apărut deficitele neurologice sau sindromul de hipertensiune intracraniană, operația trebuie făcută cât mai rapid posibil, pentru a corecta starea neurologică.
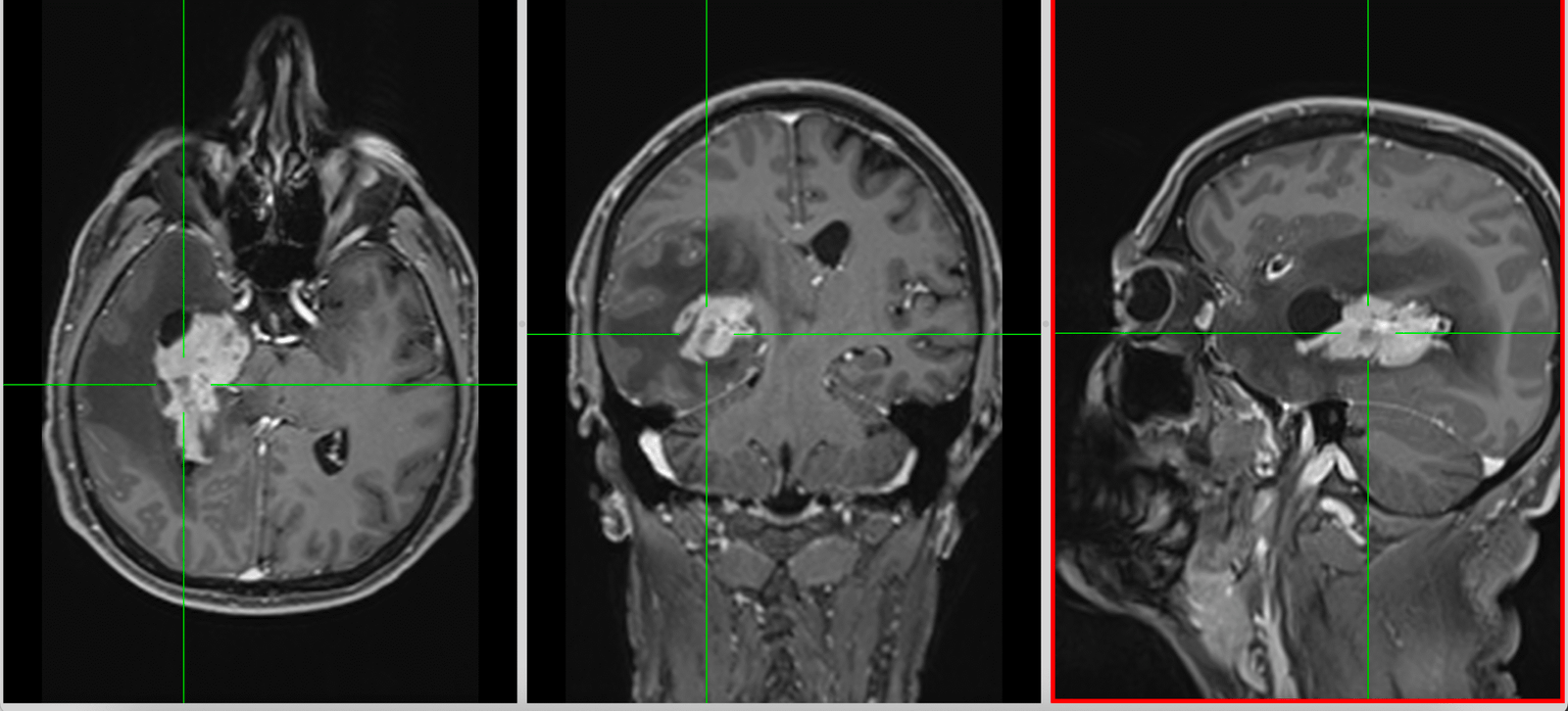
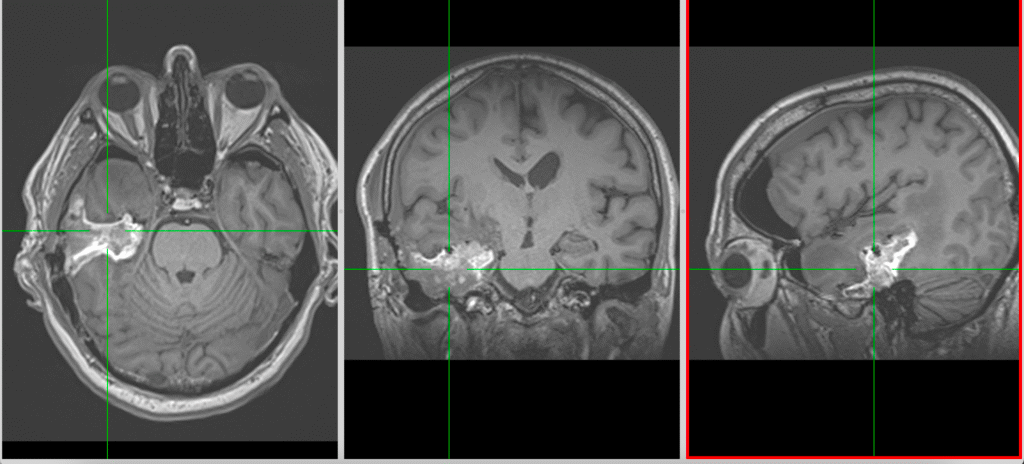
Protocol de tratament în glioblastom
DESCARCĂ SCHEMA PROTOCOLULUI PDF
Acest protocol de tratament și urmărire este dezvoltat în urma discuțiilor multidisciplinare – Neurochirurgie, Oncologie, Radioterapie, Imagistică Medicală, Anatomie Patologică și Neurologie. Protocolul este bazat pe date concrete, certe și de actualitate din literatura de specialitate.
Fiind vorba de un protocol de tratament, am inclus doar informațiile validate, pentru care există un consens la momentul actual. Terapiile alternative sau experimentale, aflate încă în studii preclinice sau clinice, dar fără confirmare până în prezent, nu pot fi acceptate momentan ca “standard terapeutic”.
În măsura în care o metodă de tratament aflată, în prezent, în studiu se va dovedi valoroasă, o vom include în protocolul nostru și o vom introduce în practică.
Etapa 1 – Diagnosticul
- Obligatoriu RMN cerebral cu contrast și protocol 3D pentru neuronavigație.
- CT cerebral cu contrast – doar la pacienții care nu pot face RMN.
Etapa 2 – Intervenția chirurgicală
- Cât mai repede de la momentul diagnosticului.
- Scop: îndepărtarea completă a tumorii fără afectarea funcțiilor neurologice.
- Mijloace: microscop operator, neuronavigație, monitorizare neurofiziologică intraoperatorie (awake surgery), fluorescență 5-ALA.
- Intervenție minim-invazivă, spitalizare minimă (3-5 zile), recuperare rapidă.
- Pacienții inoperabili – biopsie ghidată prin neuronavigație.
Etapa 3 – Controlul RMN (cu contrast)
- Primul RMN postoperator – la 24 ore de la operație.
- Al doilea RMN – la 3 săptămâni de la operație (va fi folosit și pentru planul de radioterapie).
- Al treilea RMN – la 6 săptămâni de la încheierea radioterapiei.
- Următoarele RMN – la interval de 2 luni.
Etapa 4 – Diagnosticul histopatologic
- La 7-14 zile de la operație.
- Obligatoriu și imunohistochimie, în special pentru Ki67 și IDH1.
- Teste genetice – codeletia 1p-19q, mutațiile genelor IDH1 – IDH2 și statusul de metilare MGMT. Au valoare strict prognostica si utilitatea este mai redusă pentru tumorile de grad WHO IV (glioblastom), mai utile doar pentru astrocitomul anaplazic (WHO III).
Etapa 5 – Radioterapia
- Iradierea locului fostei tumori și a țesutului cerebral din jur cu tehnici moderne IMRT – VMAT sau True Beam.
- Doza totală este de 60 Gy, fracționată în doze zilnice de 2 Gy (5 ședințe pe săptămână, 6 săptămâni).
- Se începe la aproximativ 4 săptămâni după operație, timp necesar pentru vindecarea plăgii operatorii, obținerea diagnosticului anatomo-patologic și conceperii planului de radioterapie.
Etapa 6 – Chimioterapia
- Temozolamida este citostaticul de elecție.
- Se începe odată cu radioterapia – doza zilnică (5 zile pe săptămână) pe toată durata radioterapiei.
- Monoterapia – după finalizarea radioterapiei, se administrează câte 5 doze zilnice în fiecare lună, timp de 6 luni (6 cure) sau până la constatarea recidivei sub tratament.
- Reacțiile adverse pot determina scăderea dozei sau întreruperea tratamentului.
Etapa 7 – Recidiva
- Tratamentul în caz de recidivă trebuie particularizat în funcție de situația concretă și stabilit în cadrul unei comisii multidisciplinare formate din neurochirurg, radioterapeut și oncolog.
- Reintervenția chirurgicală – atunci când recidiva este pe locul fostei tumori sau în vecinătate (nu la distanță sau în emisferul cerebral contralateral).
- Reiradierea – atunci când recidiva este la distanță, într-o zonă care nu a fost iradiată deja.
- Chimioterapia – atunci când există recidivă tumorală sub tratament cu Temozolamida, se pot folosi citostatice de linia a doua: Irinotecan, Lomustina, Bevacizumab, PCV (Proarbazina – CCNU – Vincristina), cu rezultate mai slabe și reacții adverse mai mari. Dacă au trecut mai mult de 6 luni de la ultima cură de Temozolamida, se poate reîncepe adminstrarea ei.
- Tratament paliativ – “best suportive care” pentru ameliorarea simptomelor și menținerea calității vieții în cazurile depășite din punct de vedere terapeutic.