Glioblastomul multiform – o boală a contrastelor: între progres tehnologic și limite biologice
Glioblastomul multiform (GBM) rămâne, în ciuda progreselor remarcabile ale medicinei moderne, una dintre cele mai provocatoare patologii din neuro-oncologie. Este tumora care testează simultan limitele chirurgiei, ale radioterapiei și ale terapiei sistemice, dar și capacitatea noastră de a înțelege și gestiona complexitatea biologică a creierului.
Definit în prezent, conform clasificării OMS 2021, ca astrocitom difuz de grad 4, IDH wild-type, glioblastomul nu este doar o tumoră agresivă, ci o boală difuză a creierului. Această distincție este esențială. În timp ce multe tumori solide pot fi tratate prin excizie completă, glioblastomul se dezvoltă și se extinde dincolo de limitele vizibile, infiltrând structurile funcționale ale creierului într-un mod subtil, dar constant.
Această natură infiltrativă definește întreaga strategie terapeutică și explică, în mare parte, de ce boala recidivează aproape invariabil, chiar și după tratament optim.
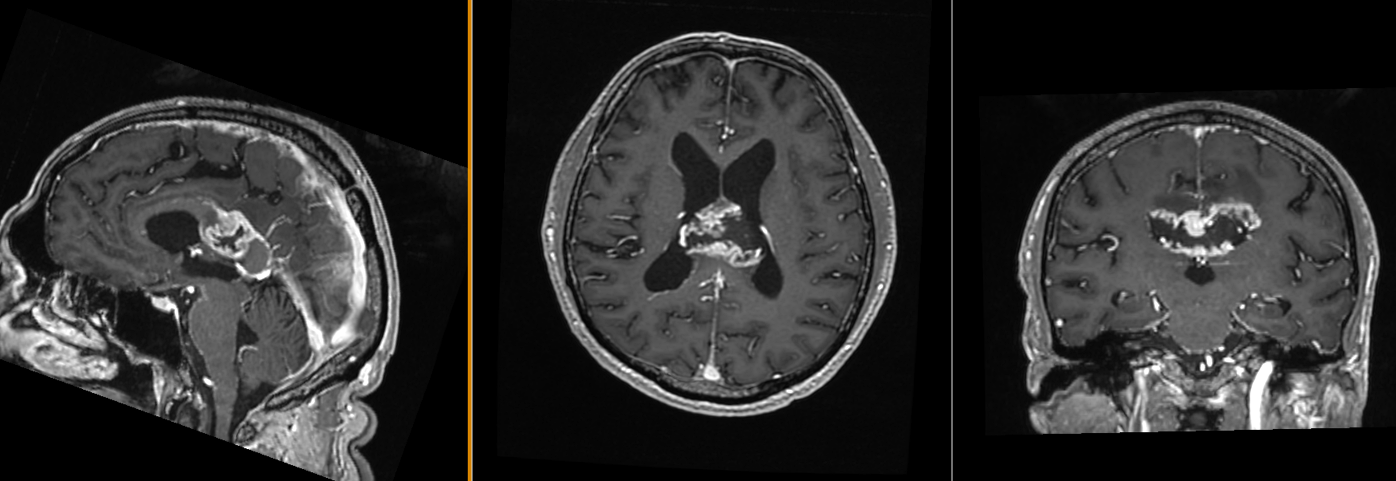
Dincolo de imagine: realitatea biologică a glioblastomului
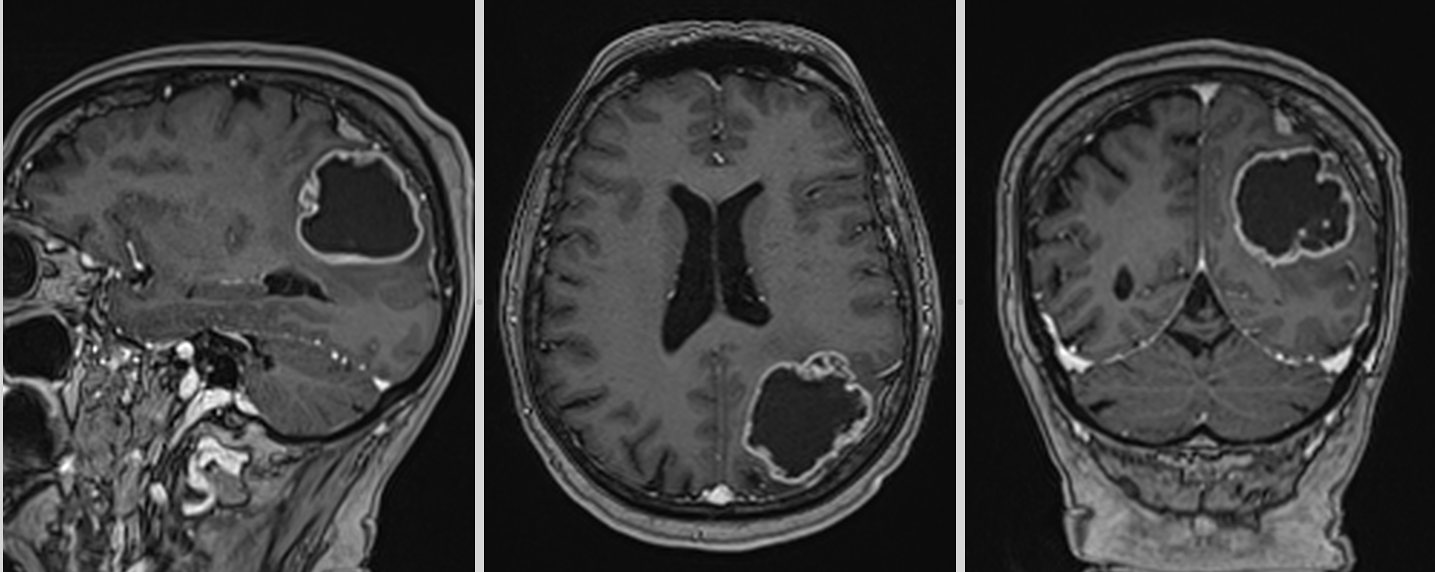
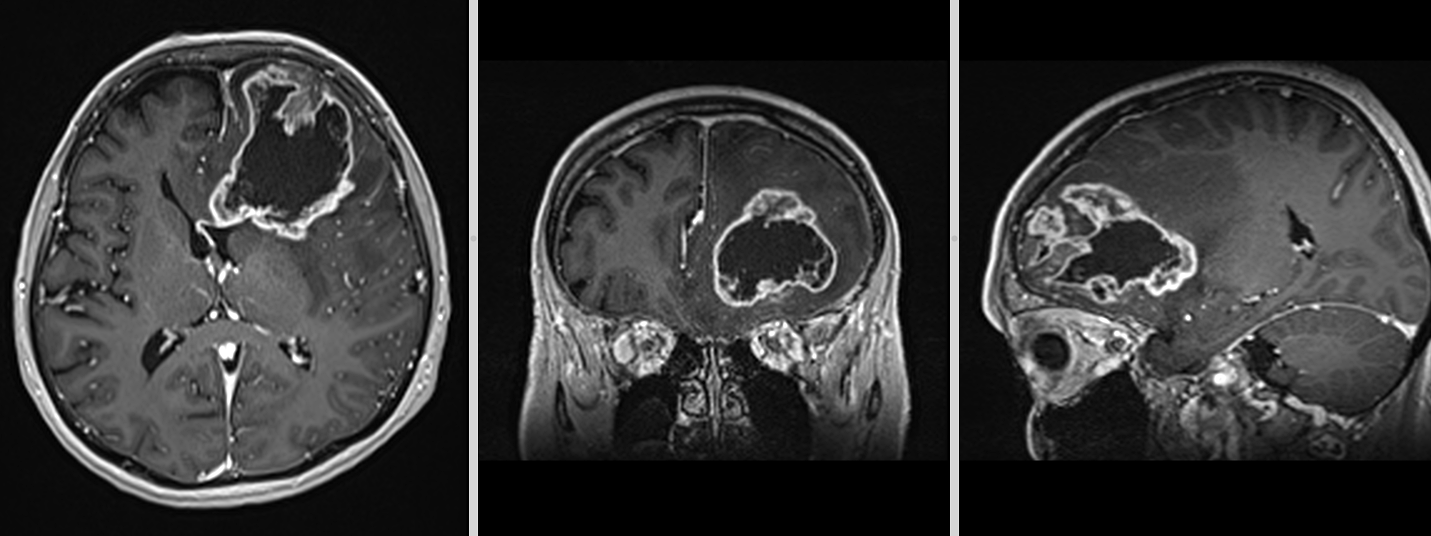
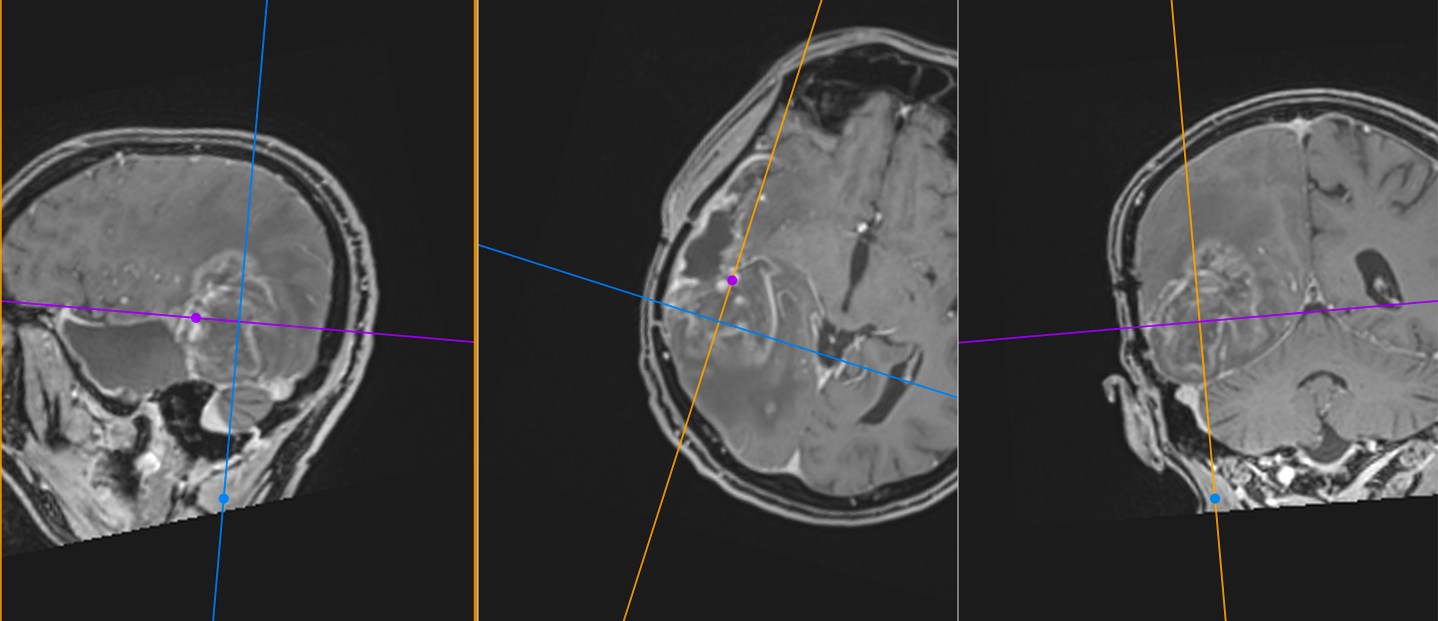
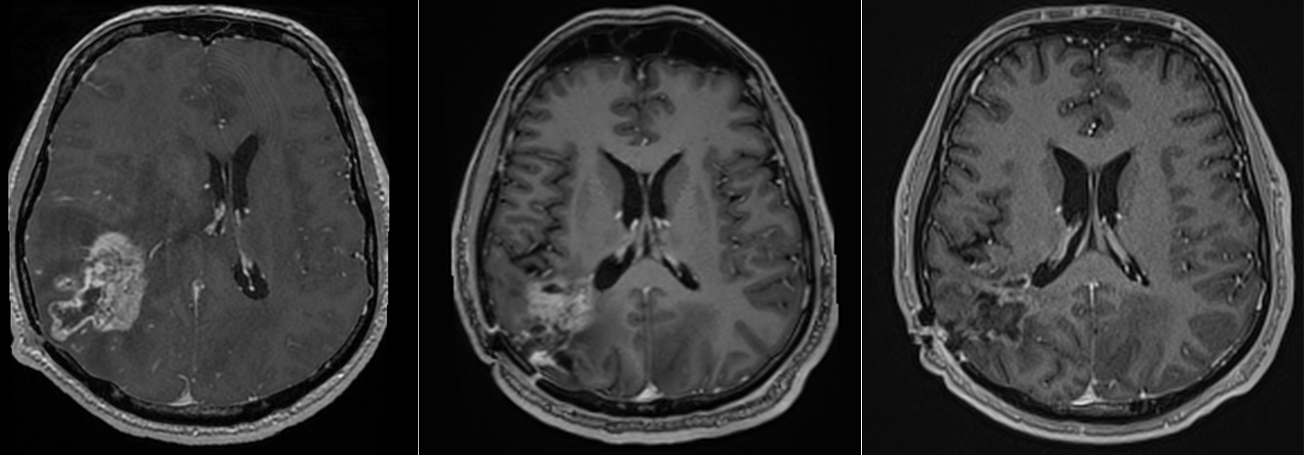
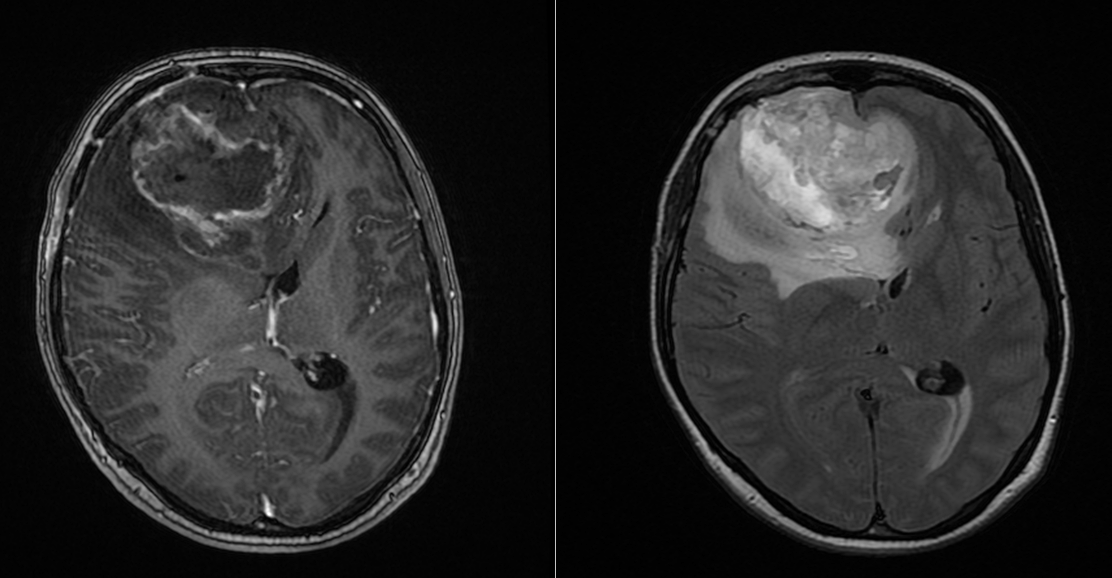
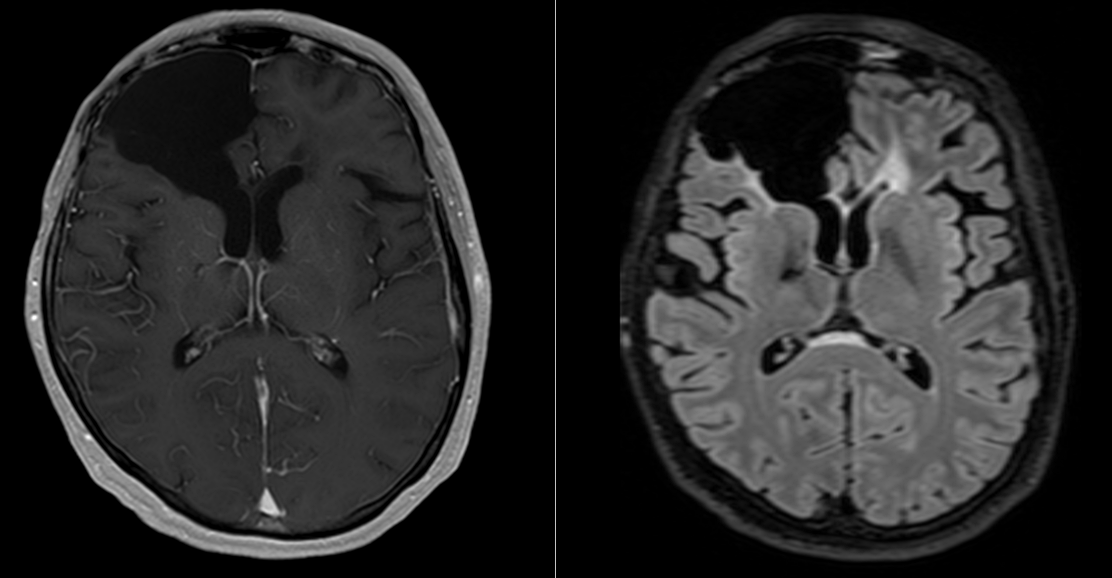
La nivel imagistic, glioblastomul apare adesea ca o leziune relativ bine delimitată, cu captare inelară de contrast și necroză centrală. Pentru ochiul neavizat, aceasta poate sugera o tumoră care ar putea fi „scoasă complet”. În realitate, ceea ce vedem pe RMN reprezintă doar componenta cea mai densă tumoral.
La nivel microscopic, celulele tumorale:
- migrează de-a lungul tracturilor de substanță albă
- infiltrează cortexul aparent normal
- utilizează spațiile perivasculare ca „autostrăzi biologice”
Studii histologice au arătat că aceste celule pot fi prezente la centimetri distanță de leziunea vizibilă. Astfel, chiar și o rezecție chirurgicală extinsă lasă inevitabil în urmă un substrat tumoral microscopic.
Această realitate transformă glioblastomul dintr-o boală locală într-una sistemică, la nivelul creierului.

Heterogenitatea tumorală – cheia rezistenței
Unul dintre cele mai importante concepte în înțelegerea glioblastomului este heterogenitatea.
Nu există două glioblastoame identice. Mai mult decât atât, nu există nici măcar o singură populație celulară într-un glioblastom. În interiorul aceleiași tumori coexistă:
- celule stem tumorale cu potențial ridicat de regenerare
- celule diferențiate cu proliferare rapidă
- subclone cu mutații distincte
Această diversitate creează un sistem adaptativ:
- tratamentul distruge anumite subpopulații
- altele supraviețuiesc și devin dominante
Rezultatul este recidiva, de multe ori cu un profil biologic diferit față de tumora inițială.
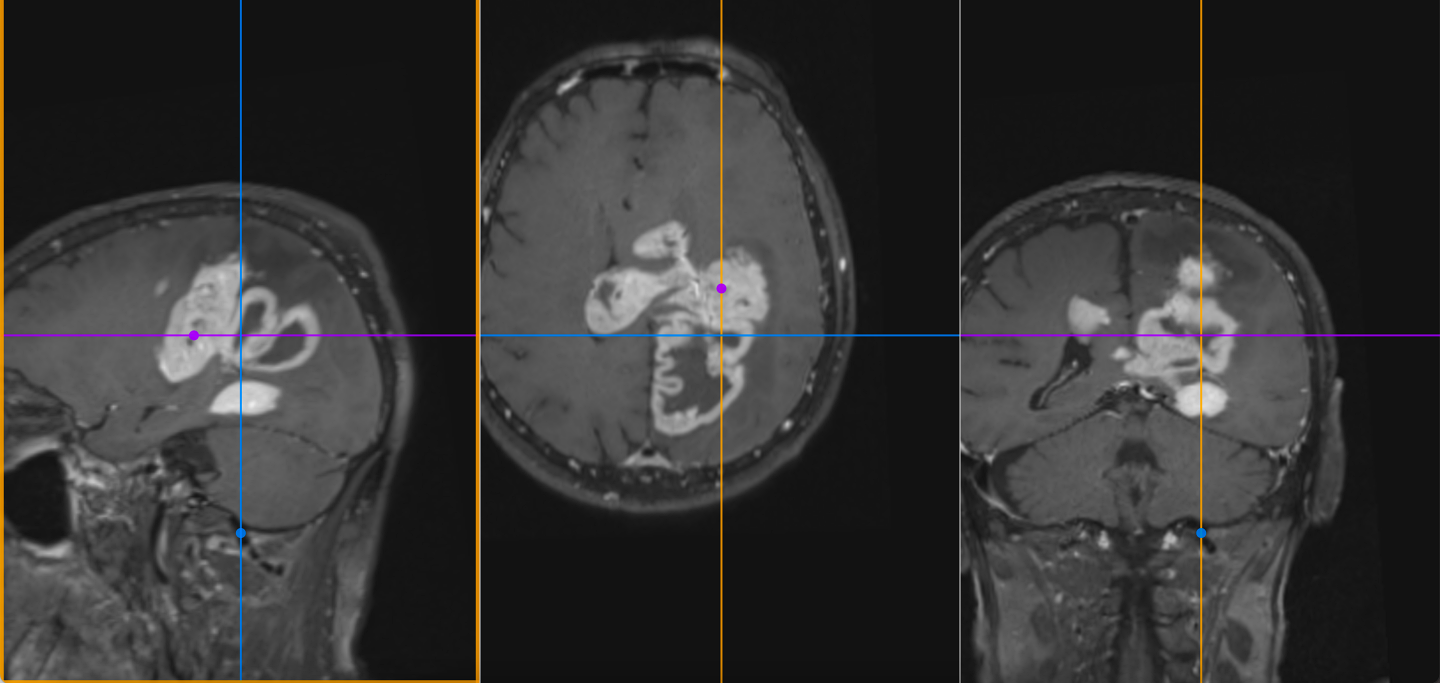
Profilul molecular – de la clasificare la decizie terapeutică
În era actuală, diagnosticul de glioblastom nu mai poate fi separat de analiza moleculară.
Caracteristicile tipice includ:
- IDH wild-type
- mutații ale promotorului TERT
- amplificare EGFR
- pierdere PTEN
- anomalii cromozomiale +7/−10
Dintre toți biomarkerii, metilarea MGMT are cea mai mare relevanță clinică. Ea influențează direct eficiența temozolomidei, fiind asociată cu o supraviețuire mai bună.
Cu toate acestea, chiar și în contextul unui profil molecular favorabil, beneficiul terapeutic este limitat în timp. Glioblastomul nu este doar o tumoră genetică, ci și una epigenetică și metabolică, capabilă să își adapteze rapid comportamentul.
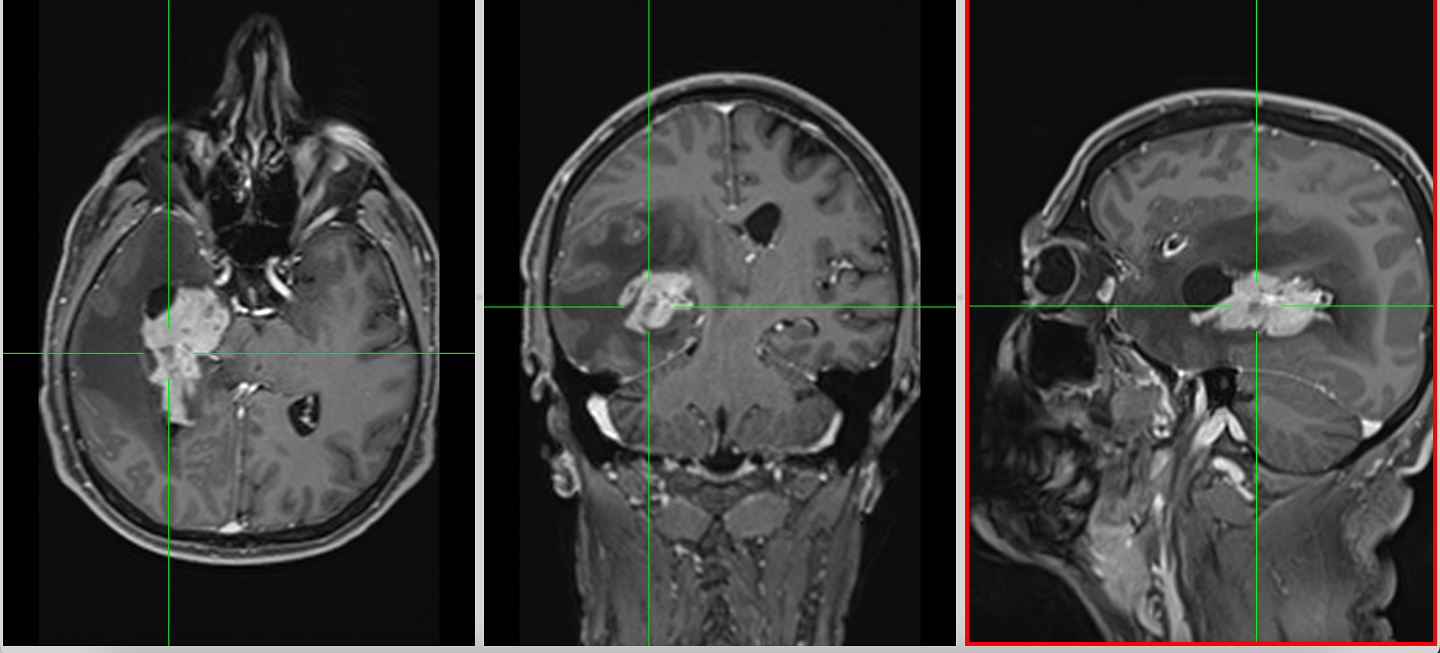
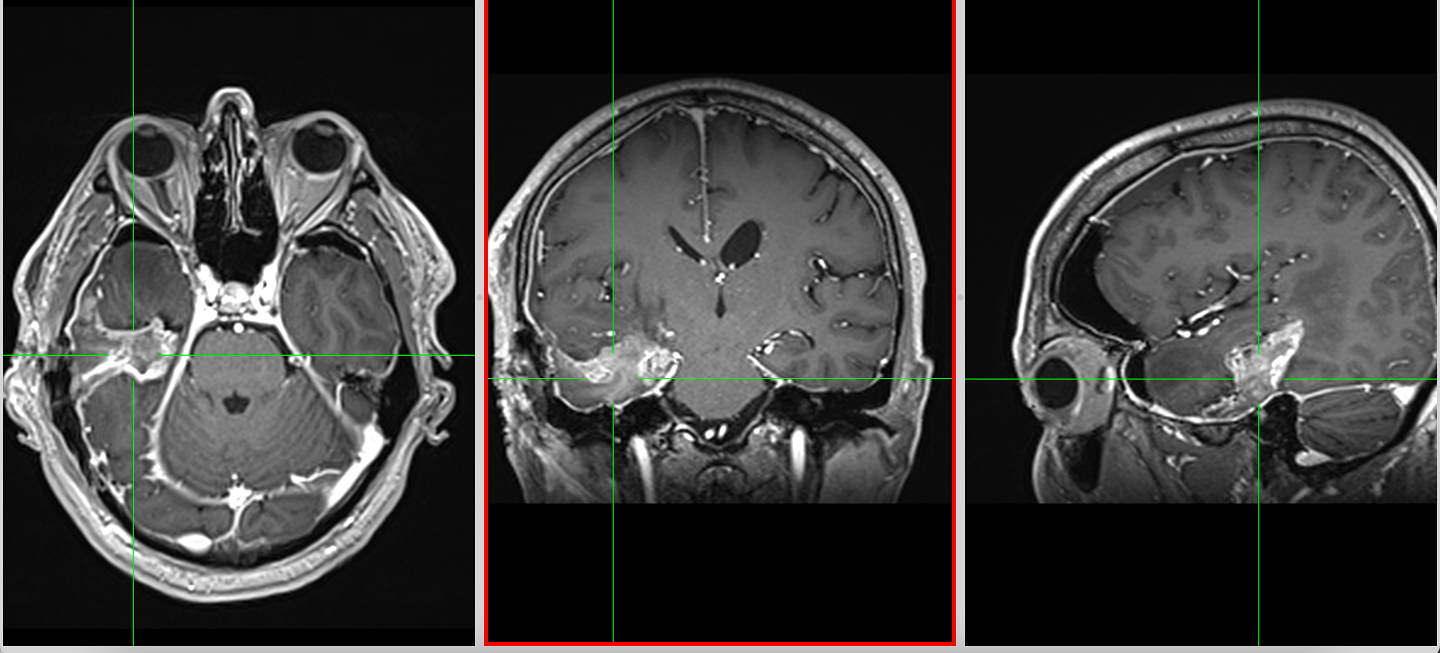
Debutul clinic – între brusc și insidios
Pentru pacient, primul contact cu boala este adesea neașteptat.
În multe cazuri, debutul este marcat de o criză epileptică. Alteori, simptomele evoluează progresiv:
- slăbiciune pe o parte a corpului
- dificultăți de vorbire
- tulburări de memorie
- modificări de personalitate
În tumorile frontale, simptomatologia poate fi subtilă, fiind interpretată inițial ca stres sau oboseală. În alte situații, deteriorarea este rapidă, reflectând creșterea accelerată a tumorii și edemul asociat.
Imagistica – instrument esențial, dar imperfect
RMN-ul cerebral este standardul diagnostic, dar trebuie interpretat în context.
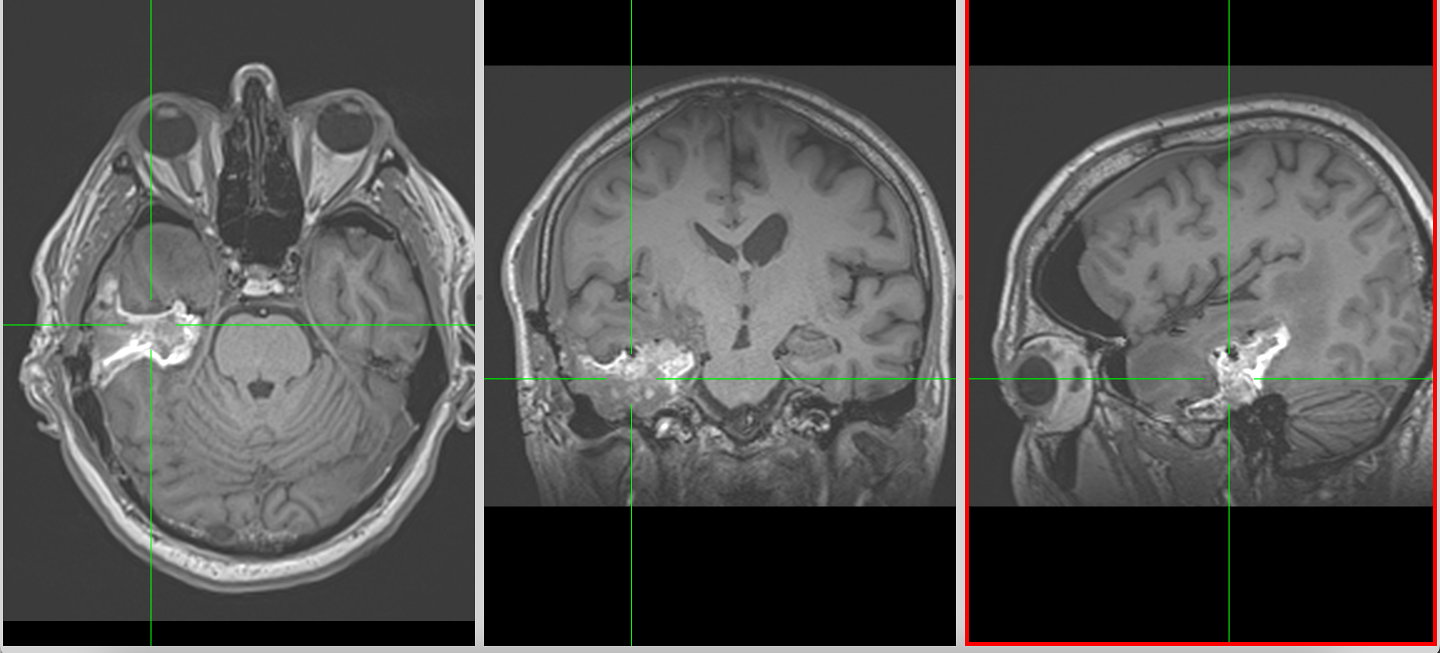
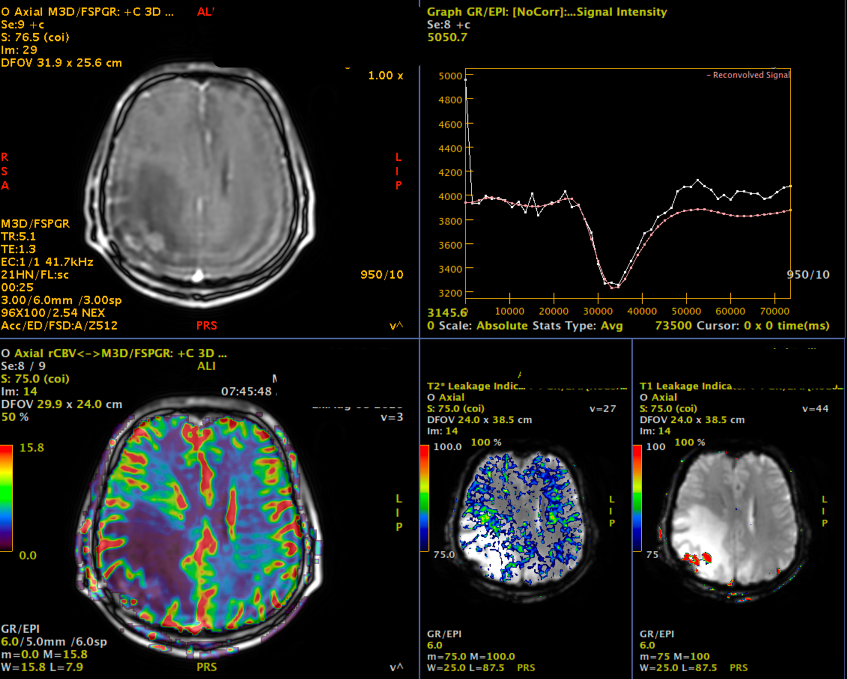
Pe lângă secvențele convenționale, tehnicile avansate aduc informații suplimentare:
- perfuzia evidențiază angiogeneza tumorală
- spectroscopia reflectă metabolismul celular
- DTI (tractografia) arată relația cu tracturile din substanța albă
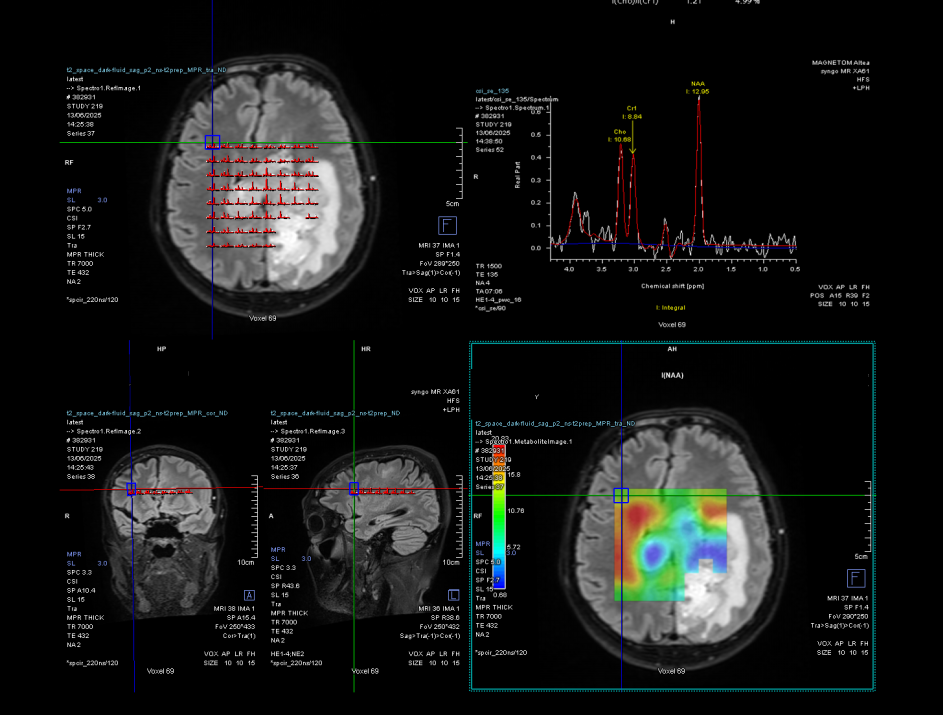
Cu toate acestea, niciuna dintre aceste metode nu poate delimita complet infiltrarea microscopică. De aceea, planificarea chirurgicală și terapeutică trebuie să țină cont de această limitare.
Chirurgia – rol central, dar nu curativ
Chirurgia reprezintă primul pas terapeutic și unul dintre cei mai importanți factori prognostici modificabili.
Conceptul actual este cel de rezecție maximală sigură, care implică:
- îndepărtarea cât mai extinsă a tumorii vizibile
- conservarea funcțiilor neurologice esențiale
Extensia rezecției este direct corelată cu supraviețuirea, însă beneficiul se pierde dacă este însoțit de deficit neurologic semnificativ.
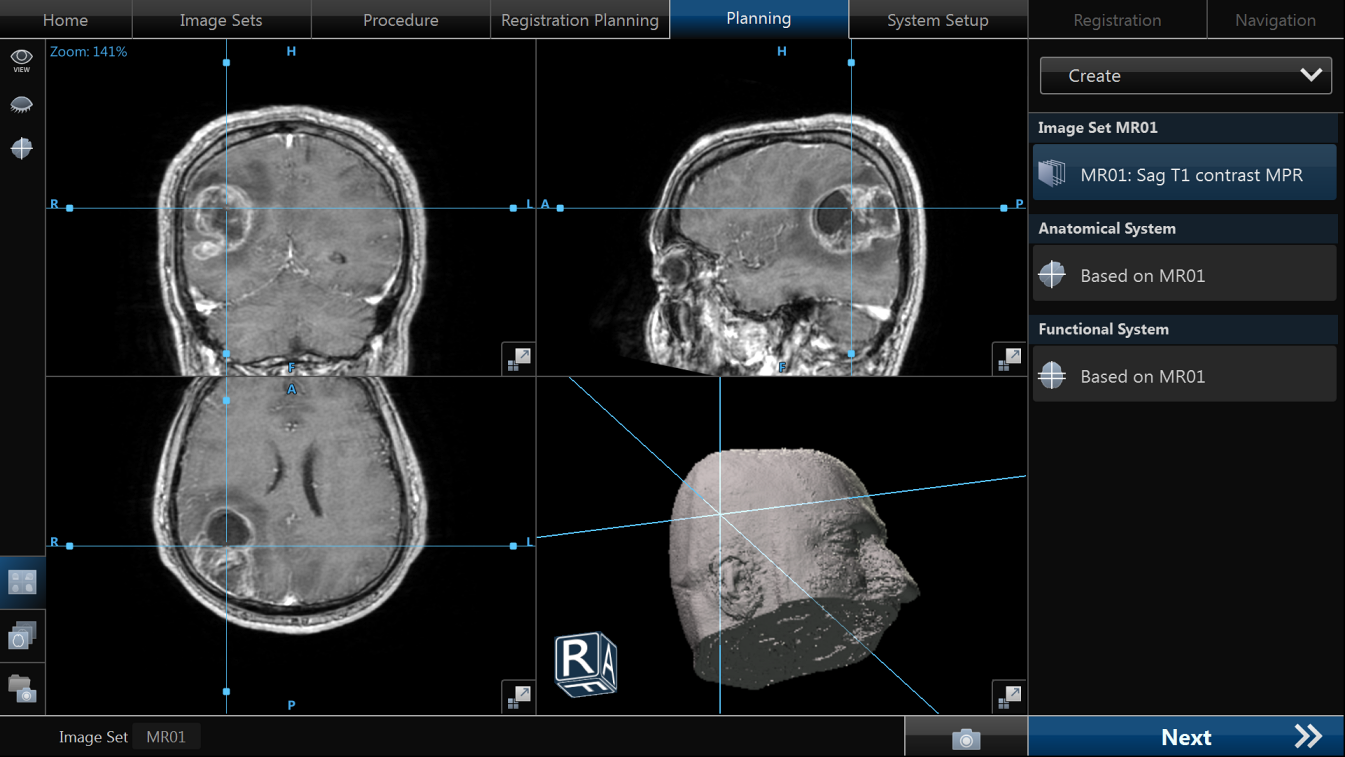
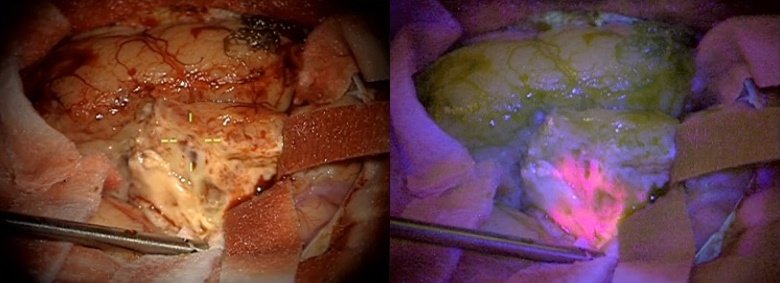
Tehnologiile moderne au crescut semnificativ siguranța:
- fluorescența 5-ALA permite identificarea țesutului tumoral activ
- neuronavigația oferă orientare spațială precisă
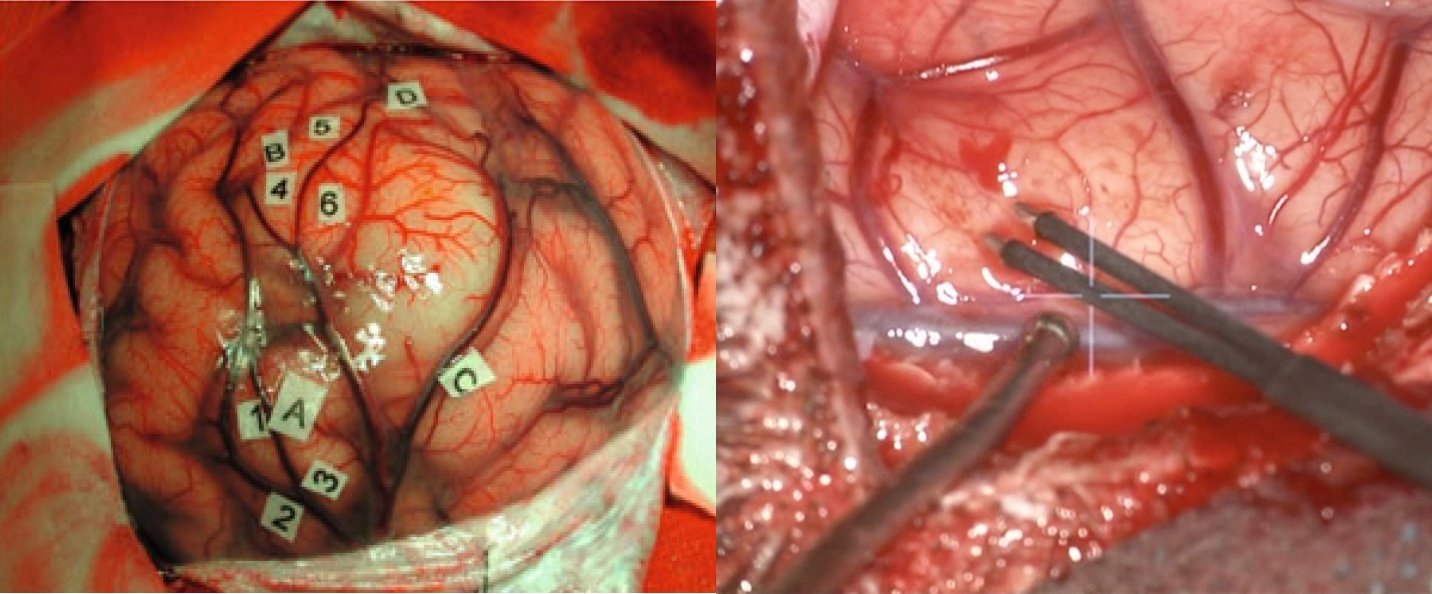
- monitorizarea neurofiziologică protejează funcțiile motorii
- chirurgia awake permite cartografierea limbajului și a funcțiilor cognitive
În practică, fiecare intervenție este o negociere fină între radicalitate și funcție.
Tratamentul adjuvant – protocolul Stupp și limitele sale
Standardul actual de tratament este reprezentat de protocolul Stupp:
- radioterapie fracționată (60 Gy)
- temozolomidă concomitent și adjuvant
Acest protocol a reprezentat un moment de referință, crescând supraviețuirea mediană la aproximativ 14–18 luni.
Cu toate acestea:
- majoritatea pacienților recidivează
- beneficiul este variabil
- rezistența tumorală apare frecvent
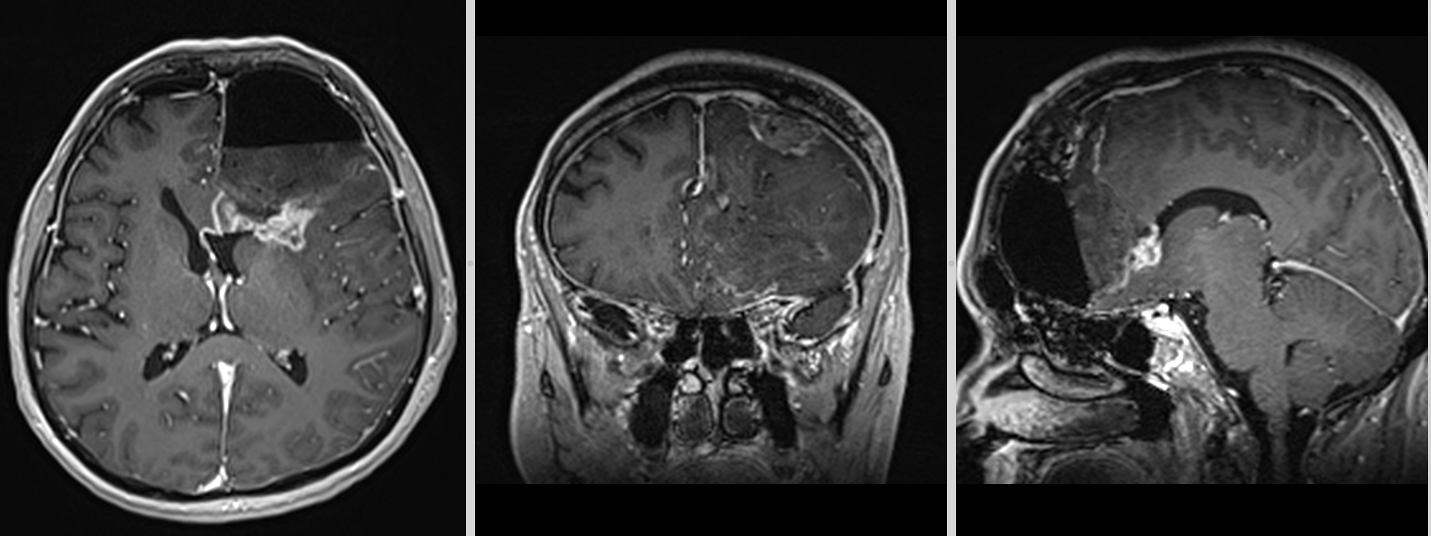
Recidiva – inevitabilitate biologică
Recidiva nu este o eventualitate, ci o etapă a evoluției bolii.
Aceasta apare de obicei:
- în vecinătatea cavității de rezecție
- rar, la distanță
La momentul recidivei, tumora este adesea:
- mai rezistentă
- mai heterogenă
- mai dificil de tratat
Opțiunile includ:
- reintervenție
- reiradiere
- chimioterapie alternativă
- studii clinice
Decizia este profund individualizată și trebuie adaptată contextului pacientului.
Terapii emergente – între promisiune și realitate
Câmpurile electrice tumorale (TTFields) au demonstrat un beneficiu modest, dar semnificativ în anumite studii, în special atunci când sunt utilizate conform protocolului.
Imunoterapia, deși revoluționară în alte tipuri de cancer, a avut până acum rezultate limitate în glioblastom. Principalele obstacole sunt:
- bariera hematoencefalică
- microambientul imun supresiv
Direcțiile actuale includ:
- vaccinuri tumorale personalizate
- terapii celulare
- combinații terapeutice
Prognostic – între statistici și realitate individuală
Datele statistice oferă repere, dar nu definesc fiecare pacient.
Factorii prognostici includ:
- vârsta
- statusul funcțional
- extensia rezecției
- profilul molecular
Cu toate acestea, evoluția individuală poate varia semnificativ.
Calitatea vieții – obiectiv esențial
În glioblastom, tratamentul nu trebuie să fie doar agresiv, ci și echilibrat.
Obiectivele includ:
- menținerea autonomiei
- conservarea funcțiilor cognitive
- controlul simptomelor
Suportul multidisciplinar este esențial:
- recuperare neurologică
- managementul epilepsiei
- suport psihologic
Dincolo de boală – pacientul
Glioblastomul nu afectează doar creierul, ci întreaga viață a pacientului și a familiei.
Deciziile terapeutice trebuie să țină cont de:
- valorile pacientului
- calitatea vieții
- obiectivele personale
În acest context, rolul echipei medicale nu este doar de a trata, ci de a ghida.
Fiecare caz trebuie analizat individual, într-un cadru multidisciplinar.
Principiile sunt:
- tratament personalizat
- utilizarea tehnologiilor moderne
- protejarea funcțiilor neurologice
- comunicare clară și empatică
Pentru că, în final, dincolo de complexitatea acestei boli, ceea ce contează este pacientul.
Protocol de tratament în glioblastom
Acest protocol de tratament și urmărire este dezvoltat în urma discuțiilor multidisciplinare – Neurochirurgie, Oncologie, Radioterapie, Imagistică Medicală, Anatomie Patologică și Neurologie. Protocolul este bazat pe date concrete, certe și de actualitate din literatura de specialitate.
Fiind vorba de un protocol de tratament, am inclus doar informațiile validate, pentru care există un consens la momentul actual. Terapiile alternative sau experimentale, aflate încă în studii preclinice sau clinice, dar fără confirmare până în prezent, nu pot fi acceptate momentan ca “standard terapeutic”.
Etapa 1 – Diagnosticul
- Obligatoriu RMN cerebral cu contrast și protocol 3D pentru neuronavigație.
- CT cerebral cu contrast – doar la pacienții care nu pot face RMN.
Etapa 2 – Intervenția chirurgicală
- Cât mai repede de la momentul diagnosticului.
- Scop: îndepărtarea completă a tumorii fără afectarea funcțiilor neurologice.
- Mijloace: microscop operator, neuronavigație, monitorizare neurofiziologică intraoperatorie (awake surgery), fluorescență 5-ALA.
- Intervenție minim-invazivă, spitalizare minimă (3-5 zile), recuperare rapidă.
- Pacienții inoperabili – biopsie ghidată prin neuronavigație.
Etapa 3 – Controlul RMN (cu contrast)
- Primul RMN postoperator – la 24 ore de la operație.
- Al doilea RMN – la 3 săptămâni de la operație (va fi folosit și pentru planul de radioterapie).
- Al treilea RMN – la 6 săptămâni de la încheierea radioterapiei.
- Următoarele RMN – la interval de 2 luni.
Etapa 4 – Diagnosticul histopatologic
- La 7-14 zile de la operație.
- Obligatoriu și imunohistochimie, în special pentru Ki67 și IDH1.
- Teste genetice – codeletia 1p-19q, mutațiile genelor IDH1 – IDH2 și statusul de metilare MGMT. Au valoare strict prognostica si utilitatea este mai redusă pentru tumorile de grad WHO IV (glioblastom), mai utile doar pentru astrocitomul anaplazic (WHO III).
Etapa 5 – Radioterapia
- Iradierea locului fostei tumori și a țesutului cerebral din jur cu tehnici moderne IMRT – VMAT sau True Beam.
- Doza totală este de 60 Gy, fracționată în doze zilnice de 2 Gy (5 ședințe pe săptămână, 6 săptămâni).
- Se începe la aproximativ 4 săptămâni după operație, timp necesar pentru vindecarea plăgii operatorii, obținerea diagnosticului anatomo-patologic și conceperii planului de radioterapie.
Etapa 6 – Chimioterapia
- Temozolamida este citostaticul de elecție.
- Se începe odată cu radioterapia – doza zilnică (5 zile pe săptămână) pe toată durata radioterapiei.
- Monoterapia – după finalizarea radioterapiei, se administrează câte 5 doze zilnice în fiecare lună, timp de 6 luni (6 cure) sau până la constatarea recidivei sub tratament.
- Reacțiile adverse pot determina scăderea dozei sau întreruperea tratamentului.
Etapa 7 – Recidiva
- Tratamentul în caz de recidivă trebuie particularizat în funcție de situația concretă și stabilit în cadrul unei comisii multidisciplinare formate din neurochirurg, radioterapeut și oncolog.
- Reintervenția chirurgicală – atunci când recidiva este pe locul fostei tumori sau în vecinătate (nu la distanță sau în emisferul cerebral contralateral).
- Reiradierea – atunci când recidiva este la distanță, într-o zonă care nu a fost iradiată deja.
- Chimioterapia – atunci când există recidivă tumorală sub tratament cu Temozolamida, se pot folosi citostatice de linia a doua: Irinotecan, Lomustina, Bevacizumab, PCV (Proarbazina – CCNU – Vincristina), cu rezultate mai slabe și reacții adverse mai mari. Dacă au trecut mai mult de 6 luni de la ultima cură de Temozolamida, se poate reîncepe adminstrarea ei.
- Tratament paliativ – “best suportive care” pentru ameliorarea simptomelor și menținerea calității vieții în cazurile depășite din punct de vedere terapeutic.